Efecto de hormonas tiroideas y hormonas esteroideas
Objetivo de aprendizaje
- Muestra al alumno la exploración de tiroides y su valoración ultrasonográfica.
- Describe la fisiología de la glándula tiroides y suprarrenal.
Resultados de aprendizaje
- Integra los mecanismos de regulación del eje hipotálamo-hipófisis-tiroides e hipotálamo-hipófisis-suprarrenal.
- Aplica los conocimientos aprendidos en resolver viñetas en sujetos con alteraciones en los ejes neuroendocrinos.
Glosario de términos
CA 125: Mide la cantidad de proteína CA 125 (antígeno del cáncer 125) presente en la sangre. Se puede hacer esta prueba para controlar ciertos tipos de cáncer durante el tratamiento y después de finalizarlo.
TC-99: El tecnecio 99m (99mTc) en forma de pertecnetato (1-2 mCi) se inyecta intravenosamente. Este ion, al igual que el ion de yoduro, es transportado activamente por el simportador de sodio y yoduro al interior del tirocito pero, a diferencia del yodo, no queda integrado en los compuestos orgánicos.
1. Introducción
- Eje hipotálamo-hipófisis-tiroides
Las hormonas tiroideas regulan la tasa a la que ocurre la fosforilación oxidativa de las células. Como resultado, establecen las tasas basales de consumo de oxígeno por el cuerpo y también de producción de calor corporal por ellos es conocida como acción termogénica de las hormonas tiroideas. La cantidad de hormonas tiroideas en sangre debe estar dentro de limites normales para que el metabolismo basal funcione a la velocidad necesaria para el aprovechamiento equilibrado de la energía.
En las etapas tempranas del desarrollo del sistema nervioso central, las hormonas tiroideas participan en la diferenciación y maduración de dicho sistema, y su ausencia condiciona un retraso en el desarrollo psicomotriz. Las hormonas tiroideas también participan en la regulación del control del crecimiento corporal, promoviendo la expresión del gen de la hormona de crecimiento. En tejidos como músculo esquelético, corazón, e hígado las hormonas tiroideas tienen efectos directos sobre la síntesis de proteínas estructurales y enzimáticas. Estas acciones se llevan a cabo a través de receptores para hormonas tiroideas que están unidos a elementos de respuesta de hormonas tiroideas en el ADN.
La unión de las hormonas tiroideas a su receptor forma un complejo llamado receptor de retinoide X, algunos de los resultados de esta unión son la activación de la transcripción, el incremento o la disminución en la producción de ARNm.
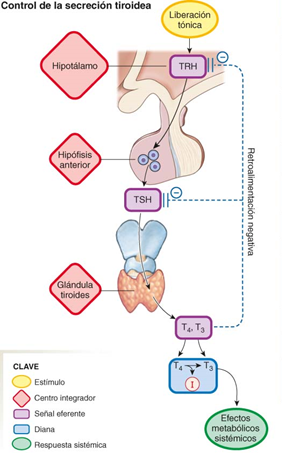
Figura 1. Eje hipotálamo-hipófisis-tiroides, se muestra la descripción de las hormonas que se involucran en la estimulación de la glándulas tiroidea y el sistema de retroalimentación negativa.
La glándula tiroidea está constituida por dos lóbulos, dichos lóbulos están constituidos por folículos, los cuales se encuentran revestidos por una capa de células epiteliales. Dentro del folículo se encuentra una sustancia proteica llamada coloide que está compuesta principalmente por tiroglobulina. El folículo tiroideo produce y secreta dos hormonas tiroideas T3 y T4, estas hormonas tienen como esqueleto dos moléculas de tirosina, las cuales están unidas por un enlace éter. La T4 tiene cuatro átomos de yodo mientras que la T3 solo tiene tres, por eso se utilizan esas abreviaturas. Las hormonas tiroideas no se secretan de esta forma normalmente, estas hormonas son producto de la escisión de tiroglobulina por medio de enzimas lisosómicas. Una vez secretadas las hormonas tiroideas al torrente sanguíneo se unen a la globulina unidora de tiroxina principalmente, aunque una pequeña cantidad de hormonas tiroideas se une a transtiretina o a la albumina. Al estar unidas las hormonas tiroideas a estas proteínas están protegidas de la inactivación metabólica y excreción renal, por consiguiente, la sobrevida de la T4 es de aproximadamente 7 días, mientras que la T3 tiene una vida media de 1 día aproximadamente.
Para la utilización de las hormonas tiroideas es necesario que la T4 se transforme en T3 que es la forma activa de estas hormonas, la proteína encargada de este proceso es la desyodasa tipo 1 que se encuentra principalmente en hígado, riñones y la propia glándula tiroides, y la desyodasa tipo 2 localizada en el músculo esquelético, sistema nervioso central, hipófisis y placenta, de esta manera las hormonas tiroideas reaccionan en receptores de hormonas tiroideas en las células objetivo. Existe una desyodasa tipo 3 que se encarga de las reacciones de degradación de las hormonas tiroideas. Cuando la concentración de T4 y T3 libres disminuye en la sangre, la hipófisis es estimulada para secretar TSH dando como resultado una mayor unión de TSH a sus receptores en las células foliculares, esta unión da como resultado la captación de yodo por las células foliculares, la yodación de las moléculas de tirosina en el precursor de tiroglobulina y en el acoplamiento de las tirosinas yodadas para formar yodotironinas. Por otro lado, la TSH al promover la síntesis de proteínas en las células parafoliculares tiroideas mantiene su tamaño y su integridad estructural. Una disminución como la hecha por una hipofisectomía produce la atrofia de la glándula, en contraste una exposición prolongada a TSH produce una hipertrofia de la glándula, generando bocio.
1.2 Eje hipotálamo-hipófisis-suprarrenal
Las hormonas esteroideas son aquellas que provienen del colesterol, dos de los órganos que se encargan principalmente de su producción son la glándula suprarrenal y las gónadas. La glándula suprarrenal está constituida por dos regiones una corteza proveniente del mesodermo y una medula que proviene del ectodermo neural. A su vez la corteza se encuentra divida histológicamente en 3 zonas, de la más externa a la más interna podemos mencionar:
- Zona glomerular, donde se produce principalmente el mineralocorticoide aldosterona.
- Zona fasciculada, que es la zona más gruesa de la corteza
- Zona reticular, que en conjunto con la zona fascicular se encargan de la producción de glucocorticoides como el cortisol y corticosterona.
Todas las zonas de la corteza producen dehidroepiandrosterona. La mayoría del colesterol que se utiliza para la síntesis de estas hormonas proviene de las lipoproteínas de baja densidad (LDL). La conversión de colesterol en las hormonas esteroideas finales depende de la participación de diversas enzimas para dar como resultado final la dehidroepiandrosterona, androstenediona, cortisol, corticosterona y aldosterona. Las hormonas esteroideas no se almacenan dentro de las células de la glándula suprarrenal, sino que su producción y por consiguiente su liberación deriva del estímulo de hormona adrenocorticotrópica (ACTH) a las células de la glándula. Una vez que se han liberado las hormonas esteroideas se unen a la globulina de unión de corticoides y a la albumina. Las hormonas que quedan en su forma libre son las que tienen efecto biológico.
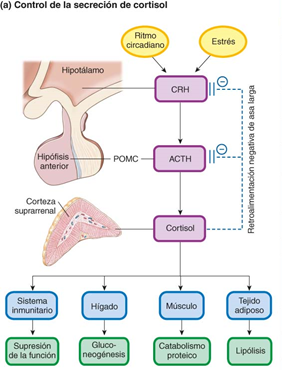
Figura 2. Eje hipotálamo-hipófisis-suprarrenal. Se muestra la relación que existe en el eje, la producción de hormonas y algunos órganos diana.
En las gónadas femeninas se produce otra hormona esteroidea de gran importancia, el estradiol. Su producción se estimula por la hormona luteinizante al estimular a la célula de la teca, igual que las otras hormonas esteroideas, la formación de los estrógenos se lleva a cabo en la mitocondria, formando como primer precursor a la pregnenolona. Para la producción de estradiol se requiere de la participación de las células de la teca y de la granulosa. Las células de la teca convierten la pregnenolona en algunos productos finales como la testosterona y androstenediona, las cuales son transformadas por la aromatasa, enzima que se encuentra en la célula de la granulosa y que es estimulada por la hormona folículo estimulante (FSH). El estradiol es de suma importancia en diversos procesos del ciclo menstrual como en la fase proliferativa del endometrio, además de mantener el sistema de conductos del sistema reproductor femenino, la persistencia de los cilios del epitelio, la movilidad de los oviductos para la adecuada movilización de los espermatozoides para llevar a cabo una fecundación. Asimismo, el estímulo que ejerce el estradiol sobre órganos como el útero, son importantes en su mantenimiento y su trofismo, de manera que una ooforectomía influye en el tamaño y el trofismo del útero.
En las gónadas masculinas, la producción de testosterona ocurre debido a que el hipotálamo libera Hormona liberadora de gonadotropina (GnRH) que estimula a las células gonadotropas para producir FSH y LH, las cuales se dirigirán al testículo unidas a globulinas trasportadoras de hormonas sexuales y ejercerán su efecto en diferentes células. La FSH en las células de Sertoli producirán inhibina que provocará una retroalimentación negativa hacia la hipófisis. La LH por otro lado provocará que las células de Leydig produzcan testosterona debido a que en estas células se encuentra presente la 17-β hidroxiesteroide deshidrogenasa, que convierte a la androstenediona en testosterona. La testosterona tiene efectos como aumento en la masa muscular, aumento en el crecimiento somático, cierre de las placas metafisarias y aumento de la espermatogénesis y la libido. Además, algunos tejidos presentan a la 5-α-reductasa que convierte a la testosterona en dihidrotestosterona que es la responsable de presentar los caracteres sexuales secundarios en los hombres.
2. Actividades en clase
2.1 Exploración de tiroides
Se anexa video de la exploración de la glándula tiroides.
https://drive.google.com/file/d/1DAx-kUUBcwcyJYHL7szfjNS2FWTWphAp/view?usp=sharing
2.2 Ultrasonido de la glándula tiroides
Sujetos y materiales: Alumno con el cuello descubierto, equipo de ultrasonido, gel para ultrasonido, sanitas.
A continuación, el docente realizará una exploración de glándula tiroidea utilizando el equipo de ultrasonido que tenemos en el laboratorio.
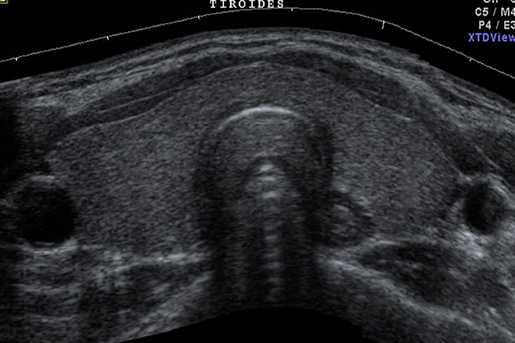
Figura 3. Imagen ultrasonográfica de la glándula tiroides.
2.3 Viñetas clínicas.
Indicaciones: Lee cada una de las siguientes viñetas clínicas, subraya lo que consideres importante del caso clínico y pregunta o investiga las palabras que desconozcas.
2.2.1. Caso 1
Paciente femenina de 49 años, antecedentes heredo-familiares relevantes con abuelo materno finado por adenocarcinoma pulmonar y una hermana finada por cáncer de mama. Antecedentes personales con tabaquismo positivo desde los 17 años consumiendo 20 cigarros al día. Niega alergias, quirúrgicos y padecer enfermedades crónicas, así como consumo de algún medicamento. Acude por presentar desde hace 2 meses con astenia, temblor fino en manos, edema distal y perdida de 27 kg de manera no intencionada. A la exploración física con peso de 41 kg, talla 159 cm, FC 112 lpm, TA 90/60 mmHg y aumento de volumen cervical con tiroides palpable con aumento de tamaño 3 veces respecto a lo normal.
Se hace el diagnóstico clínico de síndrome constitucional y bocio tiroideo en estudio.
Se le solicitan los siguientes estudios: Perfil tiroideo: TSH 0.005 μUI/mL, T4T 23.5 μg/dL, T4L >7.77 μg/dL (rango normal 0.9-1.6 μg/dL), T3T 5.56μg/dL,
Laboratorios generales: BH Hb 11.1 g/dL, glucosa 63 mg/dL, creatinina 0.49 mg/dL, Ac. Úrico 5.0 mg/dL, triglicéridos 65 mg/dL , LDL 58 mg/dL , Bilirrubina total 1.74 mg/dL , AST 24 U/L, ALT 15.5U/L, Fosfatasa Alcalina 257 U/L, albumina 3.9mg/dL, Antígeno Ca-125 1014 U/mL
Se solicitó un ultrasonido de tiroides que reportó lo siguiente: bocio difuso con aumento de la vascularidad, a la señal Doppler de manera generalizada encontrando el signo del “infierno tiroideo”, como se muestra a continuación (Figura 4):
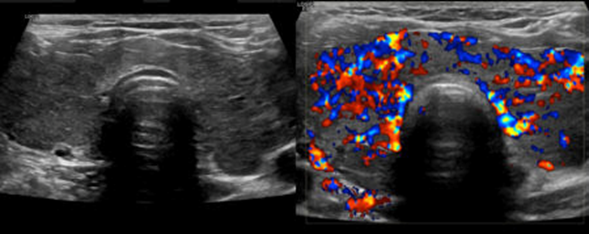
Figura 4. Imagen ultrasonográfica con Doppler mostrando el signo de “Infierno Tiroideo”
Se solicitó un gamagrama tiroideo con TC-99 que reportó aumento en la captación generalizada (Figura 5):
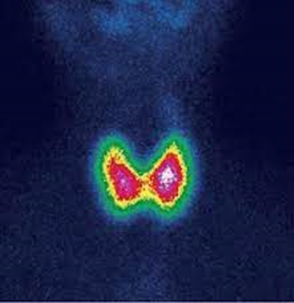
Figura 5. Estudio de gammagrafía con Tc-99 realizado a la paciente.
Con estos estudios se estableció el diagnóstico de Bocio toxico difuso o Enfermedad de Graves.
Para el control inicial de esta paciente se indicó tiamazol y propanolol.
Responde a continuación:
- ¿Esta paciente tiene algún factor de riesgo para desarrollar enfermedad de graves?
- ¿Cómo interpretarías el perfil tiroideo?
- ¿Cómo explicarías los síntomas a partir de la enfermedad diagnosticada?
- ¿Por qué se le indicaron esos dos medicamentos?
- En la enfermedad de Graves, ¿cómo se alterará el eje hipotálamo-hipófisis-tiroides?
2.2.2. Caso 2
Paciente femenina de 26 años. Antecedentes heredo-familiares relevantes, madre con tiroiditis de Hashimoto. Niega alergias, tabaquismo o consumo de alcohol. Refiere rinitis alérgica estacional con uso de antihistamínicos de manera ocasional. Niega padecer otras enfermedades crónicas o consumo de fármacos de manera rutinaria. Inicia con historia de 6 meses de alteraciones menstruales con ciclos de 45-60 días (previamente era regular) y su entrenador del gimnasio le ha comentado que no está aumentando masa muscular a pesar de adecuada alimentación y rutina de ejercicio. Ella niega astenia, fiebre, dolor o alguna otra sintomatología. A la exploración física se encuentra con peso 68 kg, talla 1.73, TA 100/80 mmHg, FC 59 lpm y resto de exploración sin relevantes, salvo a la palpación tiroidea con glándula tiroides disminuida de tamaño y con aumento en su consistencia, no dolorosa.
Se inicia el abordaje como una oligomenorrea en estudio, y se solicitan los siguientes estudios:
Química sanguínea: glucosa 79 mg/dl, creatinina 0.9, colesterol 220 mg/dL.
Perfil tiroideo: TSH 36 μUI/mL, T4T 5.6 μUI/mL, T4L 0.7 μUI/mL (rango normal 0.9-1.6 μUI/mL), anticuerpos anti-tiroglobulina 825 U/mL (rango normal <100 U/mL ), anticuerpos anti-TPO 534 (rango normal <15 U/mL).
Se realiza un ultrasonido tiroideo encontrándose disminución de tamaño de manera importante y ecogenicidad heterogénea compatible con datos de tiroiditis difusa (Figura 6):
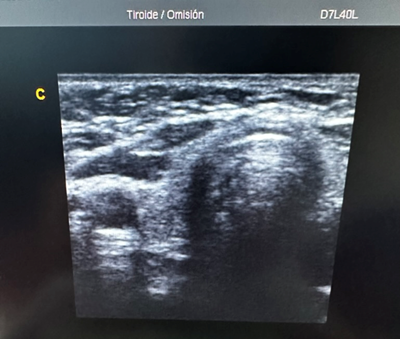
Figura 6. Ultrasonido tiroideo de la paciente.
Se establece el diagnóstico de Tiroiditis crónica autoinmune o Tiroiditis de Hashimoto y se inicia tratamiento con levotiroxina calculada a 1.6 mcg/kg de peso, además se indica que se tome en ayuno.
Resuelve las siguientes preguntas:
- ¿La tiroiditis de Hashimoto que padece la madre es relevante para la enfermedad en esta paciente?
- ¿Cómo interpretarías este perfil tiroideo?
- ¿Por qué la TSH se encuentra tan elevada?
- ¿Qué relación tiene la tiroiditis de Hashimoto con la sintomatología de la paciente?
- ¿Por qué se indicó que la levotiroxina se tome en ayuno?
- En esta paciente ¿Qué alteraciones presentará el eje hipotálamo-hipófisis-tiroides?
2.2.3 Caso3.
Paciente masculino de 37 años con antecedentes familiares de importancia, hipertensión esencial en madre y abuelo materno. Niega alergias, tabaquismo y antecedente de enfermedades crónicas. También niega consumo de fármacos o suplementos.
Inicia su padecimiento hace 3 meses con aumento de peso de 10 kg sin asociarlo a cambios en actividad física y alimentación. Se sumo presencia de hiperpigmentación en cuello y pliegues en codos y rodillas, y finalmente notó sensación de mareo al caminar y debilidad muscular, sobre todo al levantarse de la silla y subir escaleras. Por lo anterior acude a valoración médica donde se encuentra con peso 68 kg, Talla 162 cm, FC 82 lpm, TA 135/90 mmHg, A la exploración física se encuentra lo siguiente: cara de luna llena, hiperpigmentación de mucosas y presencia de acantosis nigricans, obesidad central, hipotrofia de extremidades y estrías violáceas en inglés.
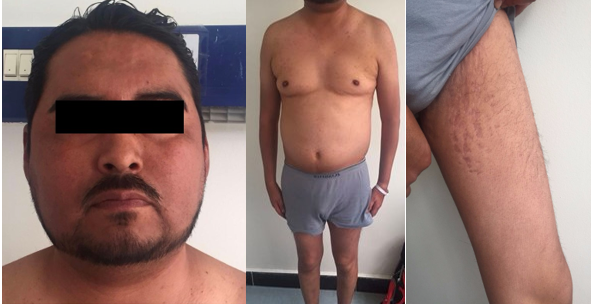
Figura 7. Exploración física del paciente.
Se inicia el abordaje como un probable síndrome de Cushing, se solicitan los siguientes estudios: Química sanguínea: glucosa 149 mg/dl, creatinina 0.92, sodio 140 mEq/L, potasio 1.9 mEq/L (rango normal 3.5-5.5 mEq/L), hemoglobina 12.7 g/dl, cortisol urinario de 24 horas 735 mcg/24 horas (normal 50-100 mcg/24 horas).
Prueba de supresión con dosis baja de dexametasona (1mg): 9.5 mcg/dl (normal <1.8 mcg/dl), niveles de ACTH 150 mcg/ml (Figura 8).
De acuerdo con el consenso en el diagnóstico (Figura 9) y tratamiento del síndrome de Cushing se realizó el abordaje.
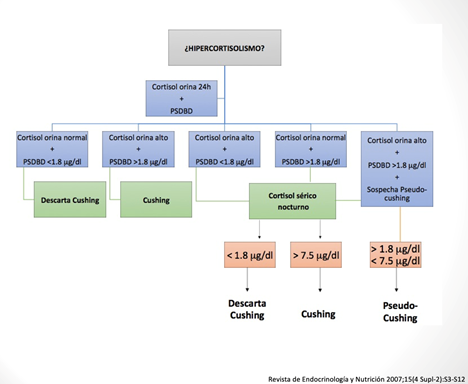
Figura 8. Pruebas de escrutinio, para demostrar el aumento en la producción de cortisol.
Prueba de supresión con dosis baja de dexametasona (PSDBD).
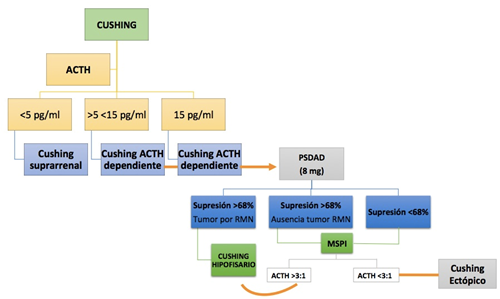
Figura 9. Pruebas de localización, se realizan después de confirmar la existencia de hipercoltisolismo.
Prueba de supresión con dosis alta de dexametasona (PSDAD)
Se realizó una prueba de supresión con dosis altas de dexametasona (PSDAD): basal 10mcg/dl, post supresión: 2.1 mcg/dl (supresión del 79%)
Posteriormente se realizó una resonancia magnética nuclear en donde se reportó: imagen coronal de silla turca en T1 donde se encuentra zona hipointensa izquierda a nivel hipofisiario compatible con microadenoma (Figura 10).
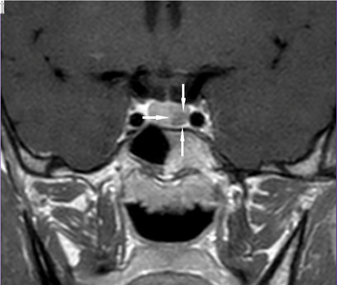
Figura 10. Microadenoma hipofisiario en una resonancia magnética nuclear.
El paciente fue diagnosticado con enfermedad de Cushing con microadenoma hipofisiario productor de ACTH y se le realizó una resección de microadenoma transesfenoidal con posterior resolución de los síntomas.
Responde las siguientes preguntas:
- ¿Cuál es la diferencia entre el síndrome de Cushing y la enfermedad de Cushing?
- ¿Por qué se mide el cortisol en orina de 24 horas?
- ¿Por qué se mide el cortisol sérico a las 8:00 en la prueba de supresión con dosis baja de dexametasona?
- ¿Cómo es el ciclo de liberación del cortisol en una persona sana?
- En la prueba de supresión con dosis alta de dexametasona, ¿Cómo se modificará el eje hipotálamo-hipófisis-suprarrenal tras administrar 2 mg cada 6 horas durante dos días seguidos?
2.2.4 Caso 4
Paciente femenina de 36 años. Antecedente familiar de madre con diagnóstico de Lupus y una hermana con Enfermedad de Graves. Niega enfermedades crónicas o consumo de fármacos. Inicia su padecimiento hace 2 meses con debilidad generalizada, mialgias, náusea y sensación de mareo constante que se exacerba al cambiar abruptamente de posición. Acude a valoración por presentar hace 48 horas síncope mientras laboraba, el cual duró 10 segundos y no se acompañó de movimientos anormales o pérdida de control de esfínteres, al despertar tuvo recuperación neurológica casi inmediata.
Al interrogatorio dirigido ha notado aumento de la coloración de su piel de manera generalizada sobre todo en cuello, brazos y encías. También refiere que no ha menstruado desde hace 4 meses con prueba de embarazo negativa. A la exploración física se encuentra peso 52 kg, talla 1.64 m, TA 70/30 mmHg, FC 119 lpm, bradilalia, hiperpigmentación en encías (Figura 11) y en cuello abarcando todas las áreas fotoexpuestas. Abdomen doloroso a la palpación. Extremidades íntegras, pero con disminución de la temperatura y llenado capilar retardado 3 segundos.
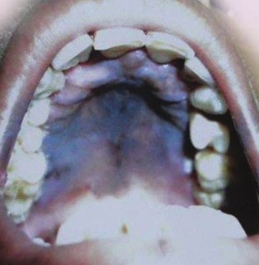
Figura 11. Hiperpigmentación en paladar y encías
Clínicamente se integran los siguientes diagnósticos: Síndrome vertiginoso, Amenorrea en estudio, Hiperpigmentación en estudio.
Como parte del abordaje diagnóstico se solicitan los siguientes estudios de laboratorio:
Química sanguínea: glucosa 59 mg/dl (normal 60-99 mg/dl), creatinina 1.3, triglicéridos 133 mg/dl, colesterol 151 mg/dl, sodio 129 mEq/L (normal 135-145), potasio 6.1 mEq/L (normal 3.5-5.5) TSH 1.4 mUi/ml, cortisol 1.3 mcg/dl (normal >15 mcg/dl), ACTH 86 mcg/ml (normal 10-40 mcg/ml).
Se realiza una tomografía de abdomen simple y contrastada. Corte transversal a la altura de glándulas suprarrenales normal (Figura 12):
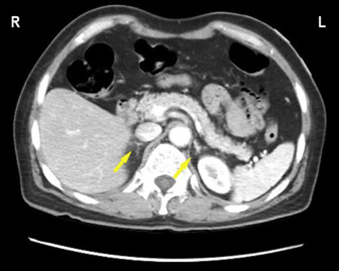
Figura 12. TAC a nivel de las glándulas suprarrenales sin evidencia de patologías.
Se establece el diagnóstico de insuficiencia suprarrenal primaria o Enfermedad de Addison, como tratamiento inicial se indica prednisona y fludrocortisona.
- ¿Qué hormonas se encuentran afectadas?
- ¿Cómo explicarías la hipotensión de esta paciente?
- ¿Cómo explicarías la hiponatremia de esta paciente?
- ¿Cuál es la causa de la hiperpigmentación de la paciente?
- ¿Por qué se le indicaron dos corticosteroides?
Referencias:
- Berne & Levy. Fisiología. 7ª Edición. Madrid: Elsevier. 2018
- Fisiología Humana. Un enfoque integrado. 8va Edición. Médica Panamericana. 2019.
- Espinosa de los Monteros-Sánchez AL, Valdivia-López J, Mendoza-Zubieta V, et al. Consenso en el diagnóstico y tratamiento del síndrome de Cushing. Rev Endocrinol Nutr. 2007;15(Suppl: 2):3-12. https://www.medigraphic.com/pdfs/endoc/er-2007/ers072a.pdf
- Nieman,L. Clinical manifestations of adrenal insufficiency in adults. En UpToDate, Rubinow, K (Ed), UpToDate. Acceso 24 de enero de 2024 https://www-uptodate-com.pbidi.unam.mx:2443/contents/clinical-manifestations-of-adrenal-insufficiency-in-adults?search=sindrome%20de%20addison&source=search_result&selectedTitle=1~150&usage_type=default&display_rank=1
Esta obra está bajo una
Licencia Creative Commons
Atribución 4.0 Internacional
Esta obra está bajo una
Licencia Creative Commons
Atribución 4.0 Internacional








Comentarios recientes